Digermyne - Digermyne

Digermynes ning og'irroq digermanium analoglari deb qaraladigan birikmalar sinfidir alkinlar. Ushbu butun sinfning ota-a'zosi HGeGeH bo'lib, u faqat hisoblash bilan tavsiflangan, ammo butun sinfning asosiy xususiyatlarini ochib bergan. Ikki Ge atomlari orasidagi katta atomlararo tortishish tufayli, faqat kinetik jihatdan barqarorlashdi digermin molekulalarini sintez qilish va katta hajmli xususiyatlar bilan tavsiflash mumkin guruhlarni himoya qilish va tegishli sintetik usullar, masalan, reduktiv birikma germaniy (II) galogenidlari.
Digerminadagi ikkita Ge atomlari orasidagi bog'lanish alkinlardagi C≡C bog'lanishidan farq qiladi, natijada trans-digerminaning egilgan tuzilishi. Trans- alkinlarning og'irroq 14-element analoglarida egilgan tuzilish juda keng tarqalgan.[1] Ikkinchi tartib Jahn-Teller Digerminlarning (SOJT) ta'siri sirpanib π bog'lanish va katta molekulyar geometrik buzilishlarni keltirib chiqaradi.
Digerminlarning ko'p qirrali xususiyati va ikkita Ge atomining katta atomlararo itarilishi, shuning uchun uzoq germaniy-germaniy masofasiga olib borishi sababli digerminlar juda reaktiv va har xil reaktsiyalarga kirishishi mumkin, masalan [2 + 1] va [2 +2] cycloaddition har xil to'yinmagan molekulalar bilan reaktsiya, [4 + 1] cycloaddition 1,3-dimetil-1,3-butadien bilan, qo'shilish reaktsiyasi alkogol va suvdan iborat bo'lib, kumush ioni bilan koordinatsion reaksiyaga kirishish uchun b-elektron donor vazifasini bajaradi.
Tayyorgarlik
Garchi ko'plab kompyuter tadqiqotlari HGeGeH ota-ona molekulasining tuzilishi va energiyasini hisoblab chiqsa ham[2][3] va organik o'rnini bosadigan digerminlar,[4] ularni katta miqdordagi R guruhlari himoyasi asosida sintez qilish va ajratish mumkin. Tegishli prekursorni, odatda germaniy (II) galogenidlarini katta miqdordagi himoya guruhlari bilan kuchli reduktantlar yordamida kamaytirish sintetik strategiyasi digerminlarni sintez qilish uchun kuchli ekanligi isbotlangan.
Germaniy (II) galogenidlarining reduktiv birikishi

Birinchi barqaror digermyne 2,6-Dipp2H3C6GeGeC6H3-2,6-Dipp2 (Ar1GeGeAr1, Dipp = 2,6-diizopropilfenil) sintez qilindi va xarakterlanadi Filipp P. Quvvat va 2002 yilda hamkasblari.[5] Katta hajmli 2,6-Dippning reduktiv birikishi2-C6H3 (Ar1) guruh bilan himoyalangan Ge (II) monoxlorid (Ge (Cl) Ar1) tarkibidagi kaliyni davolash ostida tetrahidrofuran (THF) yoki benzol Ar hosil bo'lishini berdi1GeGeAr1. C1-Ge1-Ge2-C2 yadro tuzilishi sentrosimetrikdir trans- egilgan xususiyati, C1-Ge1-Ge2 burchagi 128,67 (8) ° va ikkita Ge atomlari orasidagi masofa 2,2850 (6) Å. Ikki terefenil halqa va C1-Ge1-Ge2-C2 tekisligi o'rtasida yaxshi konjugatsiyaga ega, chunki burilish burchagi deyarli nolga teng (0,4 °). Shunga o'xshash molekula, Ar2GeGeAr2 Ar ning tavsifidan oldin hisoblab chiqilgan1GeGeAr1, optimallashtirilgan bilan trans-6 egiluvchan yadro tuzilishi yanada olomon bilan himoyalangan 2,6-Trip2C6H2 (Ar2, Trip = 2,4,6-triizopropilfenil) guruhlari.[4] Ar ichidagi trans-bükme2GeGeAr2 (123,2 °) ni Ar bilan solishtirish mumkin1GeGeAr1, va Ge-Ge masofasi 2.277 Å ham Ardan kam farq qiladi1GeGeAr1. Ar2GeGeAr2 xuddi shu qisqartirish usuli yordamida olingan[6] va Ar tuziga o'xshash tuzilishga ega bo'ldi1GeGeAr1.
Xuddi shunday sintetik usul ham Ge-Ge yagona bog'lanish bilan LGeGeL digerminin sintezini engillashtirish uchun ishlatilgan.[7] Muvaffaqiyatli uglerodli ligandlardan muvofiqlashtiruvchi atom sifatida foydalanish o'rniga, azotga asoslangan himoya guruhi L (L = N (Si (CH)3)3) (Ar3)) ishlatilgan. N-Ge-Ge ning bog'lanish burchaklari 100.09 (6) ° ga teng, ular Ar ga qaraganda ancha buzilgan1GeGeAr1 va Ar2GeGeAr2.
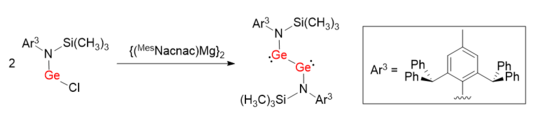
Digermilenni kamaytirish
Gavjum odamlar trans2,6-bis [bis (trimetilsilil) metil] -4- [tris (trimetilsilil) metil] fenil (Bbt) guruhlari bilan himoyalangan -dibromodigermilenni ikki ekvivalent kaliy grafit (KC) bilan kamaytirish mumkin.8) benzolda xona haroratida mos keladigan BbtGe≡GeBbt digerminini tug'diradi.[8]
Yopish
Valens aloqasi modellari
Alkinlar va digerminlar va boshqa og'ir alkin analoglari orasidagi eng aniq farq bu alkinlarda chiziqli bo'lgan molekulyar geometriya, ammo trans- barcha og'ir alkin analoglarida egilgan. Molekulyar geometriyadagi bu katta farq uglerod-uglerod uch barobar bog'lanishi va og'irroq bo'lgan 14 guruhning, masalan germaniy atomlarining ikki guruhining bog'lanishi o'rtasidagi farqdan kelib chiqadi. 14-guruh og'irroq elementlari uglerodga qaraganda ancha katta kovalent radiusga ega. Masalan, uglerodning bitta va uchli bog'lanish radiusi mos ravishda 75 Å va 60 are ga teng, germanyumning bitta va uch rishta radiusi mos ravishda 121 Å va 114 are ga teng bo'lib, ular taxminan 50% uzunroqdir.[9] 14-guruh elementlarining uchta bog'lamali REER tizimini ikkala kvartet ER fragmentlari yoki ikkita er-xotin ER fragmentlari orasidagi o'zaro ta'sir sifatida ko'rish mumkin. Avvalgi holat planar tuzilishga to'g'ri keladi, ikkinchisi esa trans- egilgan tuzilish. Kvartet ER fragmentlari energiya uglerod bo'lganida, ya'ni og'irroq 14 guruh elementlari uchun transegilgan tuzilish planar tuzilishga qaraganda energetik jihatdan afzalroq. Masalan, HGeGeH va PhGeGePh ning HGe va PhGe bo'laklari, B3PW91 / 6-311 + G (2df) (Ge uchun), 6- hisoblash darajasi bo'yicha, kvartet holatlariga qaraganda 44,2 va 44,1 kkal / mol energiyada barqarorroq. 31G (d) (C, H uchun).[10] A mezoni trans- egilgan tuzilmani CGMT modeli bilan berish mumkin.[11] Shuning uchun digerminlarda ikkita Ge atomlari orasidagi bog'lanishni valentlik bog'lanish modellari yordamida donor-akseptor o'zaro ta'siri deb ta'riflash mumkin.
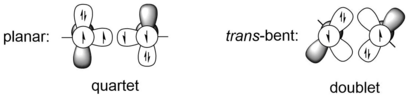
Bog'lanish tasvirlaridan ko'rinib turibdiki, Ge atomlari bitta b-bog'lanish va ikkita donor-akseptor bog'lanishlari (to'ldirilgan sp gibrid orbitalidan bo'sh p orbitaligacha) yoki bitta b-bog'lanish va bitta b-bog'lanish bilan har bir Ge atomida yakka juftlik yoki ikkita radikal aks sado beradi. Rezonans tuzilmalariga ko'ra, ikkita Ge atomining biri qisman musbat zaryadga ega va elektron etishmas, ikkinchisi Ge atomida elektron yolg'iz jufti bor va u elektron zichligini bir oz berishga qodir.

G'ayritabiiy bog'lanish burchaklari va LGeGeLning yagona bog'lanish xususiyati N atomining elektron donorlik xususiyati bilan ratsionalizatsiya qilinishi mumkin, bu esa N p (π) → Ge (bo'sh p orbital) o'zaro ta'sirining shakllanishiga olib keladi. Shuning uchun ikkita Ge atomlari orasidagi donor-akseptor bog'lanishlari zaiflashadi va ko'proq bog'lanmaydigan elektron yakka juftlariga o'xshaydi. Ge-Ge bog'lanishining bog'lanish tartibiga ma'lum darajada katta miqdordagi himoya qiluvchi guruhlarning elektron xossalari ta'sir ko'rsatishi mumkin.[8]
Molekulyar orbital (MO) davolash

Molekulyar orbital (MO) tavsifida digerminlarning geometrik buzilishi (trans-egilgan tuzilishi) ikkinchi tartib natijasidir Jahn-Teller (SOJT) effekti, bu energiyaga yaqin bo'lgan va katta molekulyar buzilishga olib kelishi mumkin bo'lgan to'ldirilgan MO (umuman digerminlardagi HOMO) bilan bog'lanmagan yoki bog'lanmagan MO (odatda ikkinchisi) o'rtasidagi o'zaro ta'sirning simmetriyasi. Agar D-da digermin molekulasini cheklash bo'lsa∞h nuqta guruhi, ikkita Ge atomlari alkininlar bilan bir xil bo'lgan past-bog'lovchi orbital, ikkita degenerat b-bog'lovchi orbital va b-antibonding orbitallar va bitta baland yotadigan b-antibonding orbital hosil qiladi. SOJT tekislikdagi bog'lash orbitalini (π) aralashtirishxBir xil b ga ega bo'lgan, HOMO) va b-antibonding orbitalsiz simmetriya trans- egilgan S2 soat nuqta guruhi, energiyasidan pastroq bo'lgan muhim bog'lanmagan elektron yolg'iz juftlik xarakteriga ega b-bog'lanishni, shuningdek, yuqori energiyaga ega b-antibonding orbitalini hosil qiling. MO ning bu ikkinchi tartibli aralashmasi geometrikadagi chiziqli D dan molekulyar buzilishlarga olib keladi∞h ga trans- egilgan S2 soat. B-bog'laydigan orbital va tekis b-antibonding orbital (π) aralashmasix*, LUMO) ham nosimmetrik (ikkalasi ham bg simmetriya) va baquvvat ravishda ruxsat berilgan. Katta SOJT effekti energiya farqi 2 eV yoki undan kattaroq bo'lgan ikki orbital o'rtasida, masalan, 4 eVda paydo bo'lishini payqab, orbitallarning aralashish darajasi alkinlarda ahamiyatsiz, ammo og'ir elementlarda, masalan, digerminlarda Ge atomlari.[12]
Reaktivlik
Cycloaddition
Digerminlarning ko'p qirrali xususiyati va ikkita Ge atomining atomlararo katta zarbasi tufayli digerminlar cycloaddition alkenlar va alkinlar bilan reaktsiyalar, masalan, etilen va asetilen.
[2 + 1] va [2 + 2] Cycloaddition
Digerminlar nisbatan to'yingan bo'lmagan kichik molekulalar, shu jumladan alkinlar, alkenlar, PhN = NPh, izosiyanidlar va azidlar bilan o'zaro nisbatan zaif Ge-Ge bog'lanishlari tufayli reaksiyaga kirisha oladi. BbtGeGeBbt etilen bilan ishlanganda ikki xil reaksiya rejimlari borligi isbotlangan, ular avval ikkalasi ham [1 + 2] sikloidlyuksiya reaktsiyasidan o'tib, germiran bilan almashtirilgan germilen oralig'ini olishadi. Germiran o'rnini bosuvchi Ge atomi keyinchalik germilenning Ge-C bog'lanishlaridan biriga osonlikcha qo'shilib, 1,2-digermatsiklobuten hosil qiladi, bu ikkala tajribada ham tasvirlangan[13] va hisoblashda.[13][14] Etilenning bosimi taxminan 1 atm bo'lgan taqdirda, 1,2-digermatsiklobuten etilenning bir ekvivalenti bilan yana o'sha sikloluksiya reaktsiyasi orqali reaksiyaga kirishib, ikkita to'rt a'zoli Ge bilan digerman hosil qiladi.2C2 ikkita uch a'zoli GeC bilan digermane esa2 uzuklar etilenning yuqori bosimi bilan olinadi. Birinchisi termodinamik barqaror mahsulot, ikkinchisi esa faqat kinetik jihatdan barqarordir, degan fikr ilgari surilgan.

Xuddi shunday, [2 + 2] tsikloduksiya reaktsiyalari digerminlar va alkinlar orasida sodir bo'ladi, masalan PhC≡CPh, 1,2-digermatsiklobutadien hosil bo'lishiga olib keladi.[15]
[4 + 1] Cycloaddition: digerminlarning diradik xarakteri

1,4-sikloheksadien hosilalarini berish uchun 2,3-dimetil-1,3-butadien bilan siklodiktsiya reaktsiyasidan o'tadigan alkinlardan farqli o'laroq, digerminlar juda reaktiv bo'lganligi sababli [4 + 1] siklodelduksiya reaktsiyasiga kirishadilar. valentlik orbital modellarida ko'rish mumkin bo'lgan diradik xarakter. Ar holatida2GeGeAr2, u 2,3-dimetil-1,3-butadien bilan reaksiyaga kirishib, g'ayrioddiy german hosilasini oladi. Reaktsiya har bir radikal markaz va 2,3-dimetil-1,3-butadien o'rtasida boshlanadi, bu [4 + 1] tsikloduksiya orqali ikkita germatsiklopent-3-ene halqalari bilan digerman hosil bo'lishiga olib keladi. Ikki GeC ning kuchaygan sterik repulsiyasi4 halqalar Ge-Ge yagona bog'lanishining gomolitik parchalanishiga olib keladi, so'ngra 2,3-dimetil-1,3-butadienning qo'shimcha ekvivalenti bilan 1,4-qo'shilish reaktsiyasi natijasida oxirgi germanani hosil qiladi.[6][15] Ge-Ge bog'lanishining uzilishi BbtGeGeBbt 2,3-dimetil-1,3-butadien bilan reaksiyaga kirishganda ko'rinmaydi, bu faqat digermanani keltirib chiqaradi.[8]
Spirtlar va suvning qo'shilish reaktsiyasi: digerminlarning ko'p bog'lanish xususiyati
BbtGeGeBbt o'tishi mumkinligi isbotlangan qo'shilish reaktsiyasi metanol va suv kabi spirtli ichimliklar bilan, o'z navbatida, digerminlarning ko'p bog'lanish xususiyatini ko'rsatadigan 1,1-dimetoksidigerman va 1,1-dihidroksidigermanani hosil qiladi.[8]

Muvofiqlashtirish reaktsiyasi

A ekanligini payqabsiz(g) digerminlarda biriktiruvchi orbital g-elektron donor Ar vazifasini bajarishi mumkin1GeGeAr1 AgSbF bilan reaksiyaga kirishishi mumkin6 hosil qilish [AgAr1GeGeAr1]+SbF6− -40 ° C da.[16] [AgAr1GeGeAr1]+ C ga ega2 CGeGeC tekisligiga va Ge-Ge bog'lanishining o'rta nuqtasiga perpandikulyar bo'lgan kumush atomi orqali o'qi. Kumush atom ikkita Ge atomlari va katta himoya guruhlarining Dipp guruhlaridan ikkita arenalar bilan muvofiqlashtiriladi. GeGe qismi va Ag o'rtasidagi bog'liqlik+ Ar ning HOMO o'rtasidagi o'zaro ta'sir ustunlik qiladi1GeGeAr1 va Ag ning 5s va 5p orbitallari+, o'zaro ta'sirning σ-xarakterini talab qiladigan, b-belgini esa Ag 4d ning nisbatan zaif o'zaro ta'siri bilan izohlash mumkin.xz π * orbital (LUMO + 1) bilan orbital. Shuning uchun, [AgAr1GeGeAr1]+ b kompleksi va metallatsiklopropenga o'xshash g kompleksi gibrididir.
Shuningdek qarang
Adabiyotlar
- ^ Kuch, Filipp P. (2010-01-14). "O'tish metallari sifatida asosiy guruh elementlari". Tabiat. 463 (7278): 171–177. doi:10.1038 / nature08634. ISSN 1476-4687. PMID 20075912.
- ^ Grev, Rojer S.; Deleeuw, Bredli J.; Sheefer, Genri F. (1990-01-12). "Germaniy-germaniyning ko'p sonli bog'lanishlari: Ge2H2 ning singleton elektron holati". Kimyoviy fizika xatlari. 165 (2): 257–264. doi:10.1016 / 0009-2614 (90) 85439-J.
- ^ Grev, Rojer S. (1991-01-01). Tosh, F. G. A .; G'arbiy, Robert (tahrir). Organometalik kimyo fanining yutuqlari. 33. Akademik matbuot. 125-170 betlar. doi:10.1016 / S0065-3055 (08) 60695-4. ISBN 9780120311330.
- ^ a b Takagi, Nozomi; Nagase, Shigeru (2001-12-01). "Germanium-germanyum va qalay-qalay qalay uch kishilik obligatsiyalarga o'rinbosar ta'siri". Organometalik. 20 (26): 5498–5500. doi:10.1021 / om010669u. ISSN 0276-7333.
- ^ Stender, Matias; Fillips, Endryu D.; Rayt, Robert J.; Kuch, Filipp P. (2002-05-17). "Alkinning Digermanium analogini sintezi va tavsifi". Angewandte Chemie International Edition. 41 (10): 1785–1787. doi:10.1002 / 1521-3773 (20020517) 41:10 <1785 :: AID-ANIE1785> 3.0.CO; 2-6.
- ^ a b Stender, Matias; Fillips, Endryu D.; Kuch, Filipp P. (2002-05-30). "[Ar * Ge {CH2C (Me) C (Me) CH2} CH2C (Me)] 2 (Ar * = C6H3-2,6-Trip2; Trip = C6H2-2,4,6-i-Pr3) hosil bo'lishi Ar * GeGeAr * ning 2,3-dimetil-1,3-butadien bilan reaktsiyasi orqali: alkinning germaniy analogining mavjudligiga dalil ". Kimyoviy aloqa. 0 (12): 1312–1313. doi:10.1039 / B203403D. ISSN 1364-548X.
- ^ Li, Djayya; Schenk, nasroniy; Gedekke, Katarina; Frenking, Gernot; Jons, Kemeron (2011-11-23). "Qattiq holatda dihidrogenni faollashtiradigan Ge-Ge yagona bog'lanishli Digermin". Amerika Kimyo Jamiyati jurnali. 133 (46): 18622–18625. doi:10.1021 / ja209215a. ISSN 0002-7863.
- ^ a b v d Sugiyama, Yusuke; Sasamori, Takaxiro; Xosoy, Yoshinobu; Furukava, Yukio; Takagi, Nozomi; Nagase, Shigeru; Tokitoh, Norxiro (2006-01-01). "Sintez va yangi kinetik jihatdan barqarorlashgan digerminning xususiyatlari: alkinning germaniy analogi uchun yangi tushunchalar". Amerika Kimyo Jamiyati jurnali. 128 (3): 1023–1031. doi:10.1021 / ja057205y. ISSN 0002-7863.
- ^ Pyykko, Pekka; Atsumi, Michiko (2009-11-23). "Li-E112 elementlari uchun molekulyar ikki tomonlama kovalent radius". Kimyo - Evropa jurnali. 15 (46): 12770–12779. doi:10.1002 / chem.200901472. ISSN 1521-3765. PMID 19856342.
- ^ Kobayashi, Kaoru; Nagase, Shigeru (1997-06-01). "Silikon − kremniy uch kishilik obligatsiyalar: O'rnini bosuvchi moddalar Disilinlarni sintetik ravishda ta'minlaydimi?". Organometalik. 16 (12): 2489–2491. doi:10.1021 / om970232f. ISSN 0276-7333.
- ^ Driess, Mattias; Grutsmaxer, Xansyorg (1996-05-03). "Karben, Olefin va kichik halqalarning asosiy guruh analoglari". Angewandte Chemie International Edition ingliz tilida. 35 (8): 828–856. doi:10.1002 / anie.199608281. ISSN 1521-3773.
- ^ Pearson, Ralf G. (1975-06-01). "Jahn-Teller effektlari to'g'risida". Milliy fanlar akademiyasi materiallari. 72 (6): 2104–2106. doi:10.1073 / pnas.72.6.2104. ISSN 0027-8424. PMC 432704. PMID 16592247.
- ^ a b Sasamori, Takaxiro; Sugaxara, Tomohiro; Agou, Tomohiro; Sugamata, Koh; Guo, Tszin-Dong; Nagase, Shigeru; Tokitoh, Norxiro (2015-09-14). "Diarildigerminning etilen bilan reaktsiyasi". Kimyo fanlari. 6 (10): 5526–5530. doi:10.1039 / c5sc01266j. ISSN 2041-6539. PMC 5510527. PMID 28757948.
- ^ Xuo, Suhong; Li, Xiaoyan; Zeng, Yanli; Zheng, Shijun; Men, Lingpeng (2013-09-01). "CH3M≡MCH3 (M = C, Si, Ge) ning C2H4 bilan reaksiya mexanizmi: [2 + 1] yoki [2 + 2] tsikloduksiya?". Molekulyar modellashtirish jurnali. 19 (9): 3501–3506. doi:10.1007 / s00894-013-1882-0. ISSN 1610-2940. PMID 23708650.
- ^ a b Kuch, Filipp P. (2005-04-01). "Alkinlarning germaniy, qalay va qo'rg'oshin analoglarini sintezi va ba'zi reaktivlik tadqiqotlari". Amaliy organometalik kimyo. 19 (4): 488–493. doi:10.1002 / aoc.824. ISSN 1099-0739.
- ^ Vang, Sinping; Peng, Yang; Olmstead, Merilin M.; Umid, Xekon; Kuch, Filipp P. (2010-09-29). "Ditetrilin b-elektron donori sifatida: [AgAr′GeGeAr ′] + SbF6− va [Ag2Ar′GeGe (F) Ar ′] + SbF6− (Ar ′ = C6H3-2,6 (C6H3-2) sintezi va xarakteristikasi , 6-Pri2) 2) ". Amerika Kimyo Jamiyati jurnali. 132 (38): 13150–13151. doi:10.1021 / ja1051236. ISSN 0002-7863. PMID 20809567.
