Nikel (II) bis (asetilasetonat) - Nickel(II) bis(acetylacetonate) - Wikipedia
 | |
 | |
| Ismlar | |
|---|---|
| Boshqa ismlar Ni (akak)2, nikel akak | |
| Identifikatorlar | |
3D model (JSmol ) | |
| ChemSpider | |
| ECHA ma'lumot kartasi | 100.019.887 |
| EC raqami |
|
PubChem CID | |
| UNII | |
CompTox boshqaruv paneli (EPA) | |
| |
| |
| Xususiyatlari | |
| C30H42Ni3O12 | |
| Molyar massa | 770.734 g · mol−1 |
| Tashqi ko'rinish | to'q yashil |
| Zichlik | 1,455 g / sm3 |
| Erish nuqtasi | 229,5 ° C (445,1 ° F; 502,6 K) (parchalanadi) |
| Qaynatish nuqtasi | parchalanadi |
| H2O | |
| Xavf | |
| GHS piktogrammalari |   |
| GHS signal so'zi | Xavfli |
| H302, H317, H334, H350 | |
| P201, P202, P261, P264, P270, P272, P280, P281, P285, P301 + 312, P302 + 352, P304 + 341, P308 + 313, P321, P330, P333 + 313, P342 + 311, P363, P405, P501 | |
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar berilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |
| Infobox ma'lumotnomalari | |
Nikel (II) bis (asetilasetonat) a muvofiqlashtirish kompleksi formula bilan [Ni (acac)2]3, bu erda akak C anionidir5H7O2− deprotonatsiyadan olingan atsetilatseton. Bu kabi organik erituvchilarda eriydigan quyuq yashil paramagnitik qattiq moddadir toluol. U suv bilan reaksiyaga kirishib, ko'k-yashil di beradiakvokompleks Ni (akak)2(H2O)2.[1]
Tuzilishi va xususiyatlari
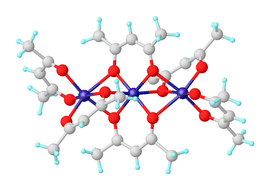
Suvsiz nikel (II) asetilasetonat Ni molekulalari sifatida mavjud3(akak)6. Uchta nikel atomlari taxminan kollinear bo'lib, ularning har bir juftligi ikki m ga teng2 kislorod atomlari Har bir nikel atomida tetragonal ravishda buzilgan oktahedral geometriya bor, chunki ular orasidagi Ni-O bog'lanishlari uzunligining farqi ko'prik va ko'priksiz oksigenlar.[2] Ni3(akak)6 molekulalari ning sentrosimmetrik bo'lmagan guruh guruhiga qaramasdan deyarli sentrosimmetrikdir cis-Ni (akak)2 "monomerlar", bu odatiy emas.[3] Trimerik tuzilish barcha nikel markazlariga oktaedr koordinatsiyasiga erishishga imkon beradi. Trimer faqat nikel markazlari juftlari o'rtasida kislorod markazlarining molekulalararo almashinuvi sodir bo'lgandagina hosil bo'ladi. Suvsiz kompleks qiziqarli magnit xususiyatlari. Taxminan 80 gachaK u odatdagi narsalarni namoyish etadi paramagnetizm 3.2 samarali magnit moment bilanmB, faqat d atrofida kutilgan momentga yaqin8 ikkita juft elektron bilan ion. Ta'sirli moment 4,1 m gacha ko'tariladiB tufayli 4.3 K da ferromagnitik almashinuv shovqinlari barcha uchta nikel ionlarini o'z ichiga oladi.[4]
Atsetilatsetonat ligandning kattaroq analoglari bilan bog'langanda sterik to'siq mononikel hosilalarining shakllanishiga yordam beradi. Ushbu xatti-harakatlar 3-metilatsetilasetonat lotinida kuzatiladi.[5]
Dihidrat

Suvsiz shaklda bo'lgani kabi, Ni (II) markazlari ham oktahedral koordinatsion joylarni egallaydi. Muvofiqlashtirish sohasi ikki bidentat tomonidan ta'minlanadi atsetilasetonat (akak) ligandlar va ikkitasi aku ligandlar. Ni (akak)2(H2O)2 cis va trans izomerlari sifatida mavjud.[6] Trans izomeriga sis izomeridan afzallik beriladi (u faqat piridin N-oksidi erituvchi sifatida ishlatilganda topilgan).[7] Trans izomerida X guruhi eksenel pozitsiyani egallaydi, etanol erituvchilarida Ni-O bog'lanishlarini hosil qiladi. Ushbu eksenel bog'lanishlar uzunligi (2.1000Å) ekvatorial Ni-O bog'lanishlaridan (2.0085 Å va 1.9961Å) kattaroqdir.[8]

Sintez
Bis (2,4-pentanedionato) nikel (II) davolash orqali tayyorlanadi nikel nitrat bilan atsetilatseton bazaning mavjudligida. Mahsulot ko'k-yashil diaquo kompleksi Ni (CH)3COCHCOCH3)2(H2O)2.[9]
- Ni (YO'Q3)2 + 2 CH3COCH2COCH3 + 2 H2O + 2 NaOH → Ni (CH3COCHCOCH3)2(H2O)2 + 2 NaNO3
Ushbu kompleksni a yordamida suvsizlantirish mumkin Din-Stark tuzog'i tomonidan azeotropik distillash:[9]
- 3 Ni (CH3COCHCOCH3)2(H2O)2 → [Ni (CH3COCHCOCH3)2]3 + 6 H2O
Subliming Ni (akak)2(H2O)2 tushirilgan bosim ostida (0,2-0,4 mm simob ustuni) 170-210 ° C da suvsiz shaklni beradi.[3]
Reaksiyalar
Suvsiz kompleks Lyuis asoslari bilan reaksiyaga kirishib, monomer qo'shimchalar beradi:
- [Ni (CH3COCHCOCH3)2]3 + 6 L → 3 Ni (CH3COCHCOCH3)2L2
Ni (akak)2(H2O)2 metin holatida yuqori rentabellikda tezda reaksiyaga kirishib, izosiyanatlardan diamidlar hosil qiladi. Bilan bog'liq reaktsiyalar dietil azodikarboksilat va dimetil asetilenedikarboksilat:
- Ni (akak)2(H2O)2 + 2 PhNCO → Ni (O2C5Men2C (O) NHPh)2 + 2 H2O
Trimer N, N-dimetilaminoetanol va kabi asoslar bilan ajralib turadi TMEDA.[10]
- [Ni (akak)2]3 + 3 chel → 3 [Ni (akak)2(chel)]
Ilovalar
Suvsiz kompleks - bu kabi nikel asosidagi katalizatorlarning kashfiyotchisi nikel bis (siklooktadien).
[Ni (akak)2]3 a kashshof yotqizish uchun NiO yupqa plyonka yordamida Supero'tkazuvchilar shisha substratlarda sol-gel texnikasi.[10]

Shuningdek qarang
Adabiyotlar
- ^ R. C. Mehrotra; R. Bohra; D. P. Gaur (1978). Metall ß-Diketonlar va ittifoqdosh hosilalar. Akademik matbuot. ISBN 0124881505.
- ^ G. J. Bullen, R. Meyson va P. Poling (1961). "Nikel (II) bisasetilatsetondagi nikelning sakkiztaral koordinatsiyasi". Tabiat. 4761 (4761): 291–292. doi:10.1038 / 189291a0.
- ^ a b G. J. Bullen, R. Meyson va P. Poling. (1965). "Bis (asetilasetonato) nikel (II) ning kristalli va molekulyar tuzilishi". Anorganik kimyo. 4 (4): 456–462. doi:10.1021 / ic50026a005.
- ^ Grinvud, Norman N.; Earnshaw, Alan (1997). Elementlar kimyosi (2-nashr). Butterworth-Heinemann. p. 1157. ISBN 978-0-08-037941-8.
- ^ 1. A. Dyringing, R. Goddard, P. W. Jolly, C. Krüger, V. R. Polyakov, "Nikel (II) ning 3-almashtirilgan Pentan-2,4-dionli hosilalarida monomer-trimer izomeriyasi", Inorg. Kimyo 1997, 36, 177-183. doi:10.1021 / ic960441c
- ^ M. Kudrat-E-Zahan, Y. Nishida va H. Sakiyama (2010). "Elektron spektrlar asosida eritmada bis (asetilasetonato) nikel (II) komplekslarining sis / trans izomerlarini aniqlash". Inorganica Chimica Acta. 363: 168–172. doi:10.1016 / j.ica.2009.09.011.
- ^ B. N. Figgis; M. A. Xitchman (2000). "Ligand maydon nazariyasi va uning qo'llanilishi". Iqtibos jurnali talab qiladi
| jurnal =(Yordam bering) - ^ O. Metin, L. T. Yildirim va S. Ozkar (2007). "Bis (atsetilasetonato) dimetanolnikel (II) ning sintezi, tavsifi va kristal tuzilishi". Anorganik kimyo. 10 (9): 1121–1123. doi:10.1016 / j.inoche.2007.06.011.
- ^ a b Vielandt, J. V.; Ruckerbauer, D. (2010). "Bis (1,5-siklooktadien) nikel (0)". Anorganik sintezlar. 35: 120. doi:10.1002 / 9780470651568.ch6.
- ^ a b Pol A. Uilyams; Entoni C. Jons; Jeymi F. Bikli; Aleksandr Shtayner; Hywel O. Devies; Timoti J. Lidxem; Syuzan A. Impey; Joanne Garsiya; Stiven Allen; Aline Rougier; Aleksandra Blyr (2001). "Ni (II) asetat va Ni (II) asetilasetonatning dimetilaminoetanol qo'shimchalarining sintezi va kristalli tuzilmalari. Elektrokromik nikel oksidli ingichka plyonkalarni sol-gel bilan biriktirish uchun kashshoflar". Materiallar kimyosi jurnali. 11 (9): 2329–2334. doi:10.1039 / b103288g.
- ^ Shrestha, Ruja; Dorn, Stefani C. M.; Veyx, Daniel J. (2013-01-16). "Alilnikel oraliq mahsulotlari orqali Enonlarga nikel-katalizli reduktiv konjugat qo'shilishi". Amerika Kimyo Jamiyati jurnali. 135 (2): 751–762. doi:10.1021 / ja309176h. PMC 3547151. PMID 23270480.
